甲状腺癌全摘出後のI-131 アブレーション・アジュバント・治療[日本甲状腺学会認定 甲状腺専門医 橋本病 バセドウ病 エコー 長崎甲状腺クリニック 大阪]
甲状腺:専門の検査/治療/知見② 橋本病 バセドウ病 甲状腺エコー 長崎甲状腺クリニック大阪
長崎甲状腺クリニック(大阪)では、甲状腺癌全摘出後のヨード131(I-131 )アイソトープ(放射線)治療を行っておりません。セカンドオピニオンも、お断りしています。
甲状腺専門の長崎甲状腺クリニック(大阪府大阪市東住吉区)院長が海外・国内論文に眼を通して得た知見、院長自身が大阪市立大学(現、大阪公立大学) 代謝内分泌内科で得た知識・経験・行った研究、日本甲状腺学会 年次学術集会で入手した知見です。
長崎甲状腺クリニック(大阪)以外の写真・図表はPubMed等において学術目的で使用可能なもの(Creative Commons License)、public health目的で官公庁・非営利団体等が公表したものを一部改変しています。引用元に感謝いたします。尚、本ページは長崎甲状腺クリニック(大阪)の経費で非営利的に運営されており、広告収入は一切得ておりません。
甲状腺・動脈硬化・内分泌代謝に御用の方は 甲状腺編 動脈硬化編 甲状腺以外のホルモンの病気(副甲状腺/副腎/下垂体/妊娠・不妊など) 糖尿病編 をクリックください。
Summary
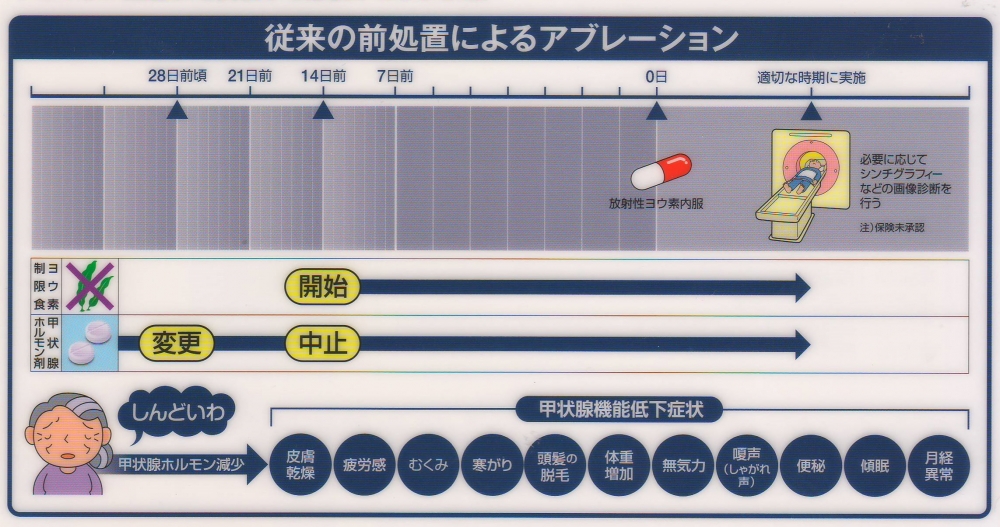
放射性ヨウ素内用療法は①アブレーション;正常な残存細胞破壊、I-131シンチグラフィーも兼ねる。1,110MBq(30mCi)、外来で可能②アジュバント治療(補助療法);再発予防、30 mCi以上100-150 mCi③放射線治療;大量100-200 mCi。I-131 放射線治療は治療前3週間から厳重なヨード(ヨウ素)制限。若年者甲状腺分化癌(乳頭癌・濾胞癌)の微細肺転移に有効、高齢者、大結節状肺転移・骨転移、低分化癌は有効性低い。2/3は放射線抵抗性でI-131が転移巣に取り込まれても縮小するとは限らない。BRAF V600E変異やRET遺伝子再配列が関与。放射線外照射の併用も。
治療約1カ月前から放射線治療専用個室退出、最後のI-131 シンチグラフィーまで甲状腺ホルモン剤(チラーヂンS)中止するため甲状腺機能低下症で心不全・うつ悪化、腎機能低下(低ナトリウム、高カリウム血症、放射性ヨウ素排泄遅延で被ばく量増加)。有害事象は唾液腺障害、嘔気と嘔吐、反回神経麻痺、永続的不妊、甲状腺クリーゼ、汎血球減少。
keywords
アブレーション,ヨウ素制限,I-131,放射性ヨウ素,甲状腺分化癌,乳頭癌,濾胞癌,放射線抵抗性,アジュバント,放射線治療
甲状腺ホルモンを合成する正常細胞(甲状腺濾胞細胞)と同様に、甲状腺分化癌(乳頭癌・濾胞癌)がヨード(ヨウ素)を取り込む性質を利用して、放射性ヨウ素(I-131)を癌細胞に取り込ませ、放射線(ベータ線)により破壊します。ベータ線は体内では1mm以下の距離しか届かず、癌細胞のみを死滅させます。
しかし、甲状腺癌細胞のヨウ素(ヨード)取り込み能力は、正常甲状腺細胞の1/10~1/100程度しかないので、正常な甲状腺組織が残っていると放射性ヨウ素(I-131)は正常甲状腺細胞にだけ集まり、甲状腺癌細胞に取り込まれません。
よって、甲状腺全摘手術した後で、甲状腺癌細胞しか残っていないのが、放射性ヨウ素(I-131)治療を行う条件です。
具体的には、甲状腺全摘手術後に放射線治療専用のRI治療病室に入院し、放射線を出すヨード(放射性ヨード、I-131)カプセルを飲むだけです。
現在、日本の放射性ヨウ素(I-131) 内照射は、日本内分泌外科学会・日本甲状腺外科学会編集の「甲状腺腫瘍診療ガイドライン2024」(2024年の改訂版)に乗っ取って行われています。同ガイドラインと「米国甲状腺学会(ATA)ガイドライン2025」では、「低リスク甲状腺癌に対する放射性ヨウ素(I-131) 内照射は原則不要」とされます。
2018年の改訂ガイドラインでは、放射性ヨウ素内用療法を3分類し
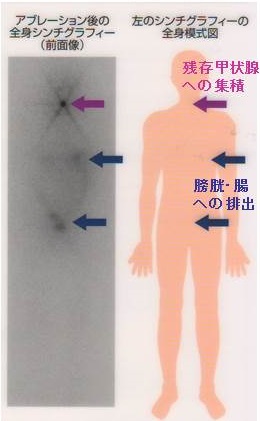
- アブレーション(ablation);甲状腺床など正常な残存細胞を完全に除去して、癌細胞がI-131 を取り込める環境を作る。I-131 シンチグラフィーも兼ねる。1,110MBq(30mCi)ほどなので、外来でも可能。[Thyroid. 2016 Jan;26(1):1-133.]
- アジュバント治療(補助療法:adjuvant therapy);従来はアブレーションと呼ばれていたものです。画像診断では確認できないが、顕微鏡的な微少残存病巣が存在すると考えられる状況で、再発予防のため行われるのを「アジュバント治療」と定義。今後は再発予防のために行うI-131 投与をアジュバント治療と言わねばなりません(混乱が生じるだけと思います)。
1,110MBq(30mCi)以上の放射性ヨウ素(I-131)が必要となります。高リスク群における転移巣・残存病変の診断(I-131 シンチグラフィー)と再発予防[無再発生存期間(RFS)の延長]目的で、アブレーション治療の3倍量以上の放射性ヨウ素(I-131)投与が推奨されています[100-150 mCi[3,700-5,550 MBq](腎障害があれば少量)]。
- 治療(treatment、放射線治療);画像上、残存腫瘍や遠隔転移が存在する場合。放射性ヨウ素(I-131) 投与量は大量100-200 mCi(腎障害があれば少量)。
ただし、分子標的薬の出現によって、最終的な治療から中間的な治療に変わった
同ガイドラインでの適正投与量は3,700-5,550MBq(100-150mCi)とされます。
外来で行われるI-131 アブレーション治療(アジュバント治療になるか?)
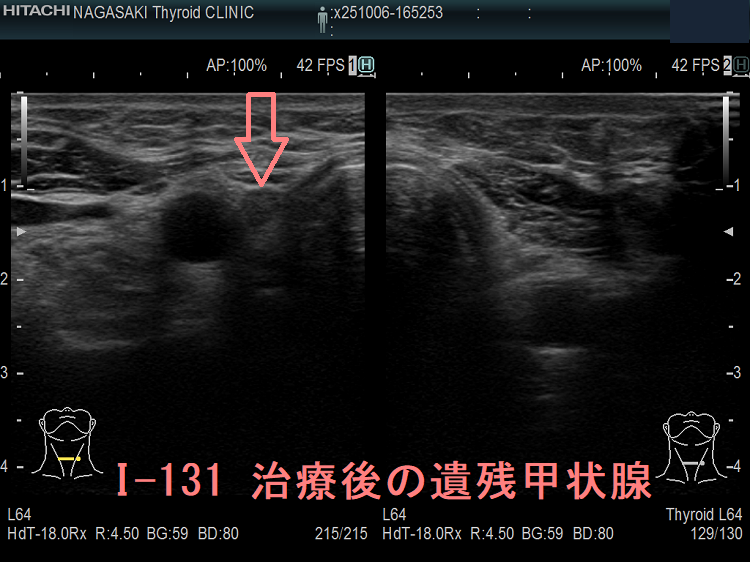
甲状腺分化癌(乳頭癌・濾胞癌)全摘手術後は、甲状腺床(甲状腺をはく離した部位)の残存細胞を完全に消滅させるため30mCi(1,110MBq=1.1GBq)のI-131 アブレーション治療を外来で行う場合があります[残存甲状腺破壊を目的としたI-131(1,110MBq)による外来治療実施要綱]。
正常甲状腺細胞が完全に消滅し、サイログロブリンを産生するのは甲状腺癌だけになるため、腫瘍マーカーとしての血清サイログロブリン値の解釈が容易になり、術後の再発診断に役立ちます。
ついでに甲状腺癌遠隔転移の診断シンチも兼ねます(I-131 シンチグラフィー)が、遠隔転移巣を破壊するには、その3倍以上の放射線量が必要です(もちろん入院で)。
ただし、外来で行う条件として、
- わかっている遠隔転移がないこと(既に肺・骨転移が見つかっている場合は不可)
- 自宅に妊婦や幼児がいないこと
- 放射性ヨウ素(I-131)服用後は直接自宅に帰ること
があります。
同時にアジュバント治療(補助療法:adjuvant therapy)として、微少残存病巣を破壊し、再発予防までできれば良いのだが、30mCiでそれが可能か不明です。
改訂「甲状腺腫瘍診療ガイドライン」では、高リスク患者に限り3.7-5.6GBq(100-150mCi)のアジュバント治療が推奨されますが、外来ではできません。
北光記念病院の報告では、遠隔転移の無い中~高リスクの甲状腺分化癌全摘出後に外来で30mCi のI-131 アジュバント治療行い、80%以上が完全寛解し、完全寛解後の再発率は15%以下だったそうです。(第62回 日本甲状腺学会 O5-1 30mCiのI-131は甲状腺癌に対するadjuvantとして適当か)
再発制御を目的としたI-131 アジュバント治療(補助療法)
中~高リスクの甲状腺分化癌(乳頭癌・濾胞癌)・低分化癌全摘出後に、再発制御を目的としてI-131 アジュバント治療(補助療法)が行われます。当然ながら、遠隔転移が見つかりI-131 放射線治療に移行する場合もあります。
大阪市立大学(現、大阪公立大学) 内分泌外科では、I-131 放射線治療に移行した人を除けば、30-150(中央値60)mCiの投与量でした(外来では30mCi まで、それ以上は放射線治療専用個室にて)。約6年間の観察で
- 甲状腺分化癌(乳頭癌・濾胞癌)・低分化癌全摘出後からI-131 アジュバント治療までの期間が1年以上と長い場合、有意に再発が多くなる。(要するに、やるなら時期を逃さず早急におこなうべき)
- 79%で無再発生存が得られる。
甲状腺分化癌(乳頭癌・濾胞癌)・低分化癌全摘出後、1年以内にI-131 アジュバント治療を行えば、早期再発が抑えられる可能性は高くなります。(第62回 日本甲状腺学会 O5-2甲状腺癌に対する放射性ヨウ素内用による補助療法の検討)
また、2023年の京都大学の報告によると、投与量1110, 1850, 3700 MBq(30, 50, 100mCi)を用いて3年後無再発生存(RFS)率は85.8% ですが、甲状腺乳頭癌以外の甲状腺濾胞癌、低分化型甲状腺癌は予後不良になります。 [Sci Rep. 2023 Jul 4;13(1):10795.]
メイヨークリニックの報告[World J Surg. 2002 Aug;26(8):879-85.]によると、最初の手術で完全に切除された限局性甲状腺乳頭癌にI-131 アジュバント治療を行った結果、
- 累積再発率は、術後5年で8%、10年で11%、40年で13%
- 再発の80%以上は最初の10年間に発生
甲状腺ホルモン剤(チラーヂンS)休薬
治療(treatment、放射線治療)では、放射性ヨウ素(I-131) 投与の4週間前(2週間前の施設もあり)から甲状腺ホルモン剤(チラーヂンS)を中止して甲状腺機能低下症にします。下垂体からのTSH(甲状腺刺激ホルモン)分泌は最大限に上昇(血清TSH濃度≧30 μIU/mLが好ましい)。甲状腺癌細胞が残っていれば、TSHに反応して放射性ヨウ素(I-131)を取り込みます(集積する)。
甲状腺機能低下に伴って心不全・うつ症状悪化、腎機能低下(低ナトリウム血症、高カリウム血症)による放射性ヨウ素(I-131)の排泄遅延と被ばく量増加がおこります。甲状腺ホルモン剤(チラーヂンS)を再開してもすぐには回復しません。
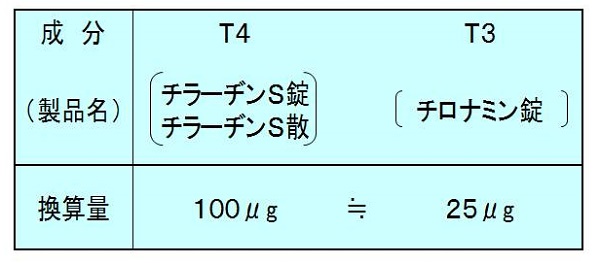
施設によっては、LT4剤(チラーヂンS)休薬に合わせてLT3剤(リオチロニン、チロナミン錠®)へ切り替える方法を採用しています。LT3は2-4時間で血中濃度が上昇するため即効性があり、血中半減期は約 1 日と短いため、I-131 投与の数日前まで服薬可能。(J Clin Endocrinol Metab. 2012 Jul;97(7):2256-71.)(Crit Care Med. 1983 Feb;11(2):99-104.)。
ただし、LT3は直接心臓に作用するため、特に高齢者で心毒性(不整脈、狭心症・心筋梗塞誘発)の危険があります。一方で、それら心毒性が出現したなら、すぐに減量できる利点もあり、諸刃の剣です(Rev Endocr Metab Disord. 2003 May;4(2):137-41.)。
ヨード(ヨウ素)摂取制限
I-131 シンチグラフィーと同じく、できるだけ多くの放射性ヨウ素(I-131)を甲状腺癌細胞に取り込ませるため、治療前3週間(2週間の施設もある)から、少なくともI-131 カプセル内服後1週間、できれば放射線治療専用個室を退室するまで徹底したヨード(ヨウ素)制限を行います。[I-131 シンチグラフィーのヨード(ヨウ素)摂取制限]
大量(100-200 mCi)のI-131 投与
放射線治療専用個室に入院して、大量(100-200 mCi)の放射性ヨウ素(I-131) 投与(腎障害があれば少量)。I-131 シンチグラフィーもついでに行う。
I-131 放射線治療の効果として、
- 若年者の甲状腺分化癌(乳頭癌・濾胞癌)の微細な肺転移には有効ですが、
①高齢者(初回I-131 治療時年齢55歳以上)
②大結節状の肺転移(転移巣1cm以上)
③骨転移、脳転移
④初回I-131 治療時の血清サイログロブリン値 400 ng/mL以上(癌細胞量が多い)
⑤乳頭癌型・濾胞癌型低分化癌
には有効性が低い。[2015 American Thyroid Association Management Guidelines. Thyroid. 2016 Jan;26(1):1-133.]
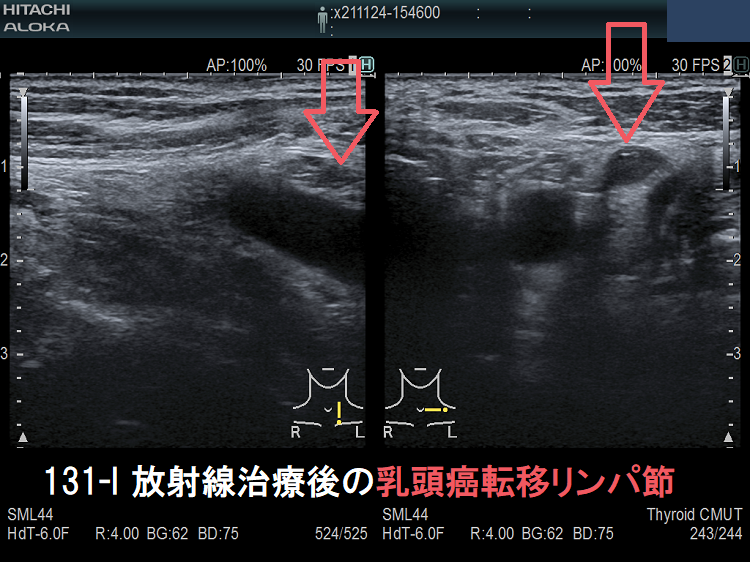
- I-131 放射線治療において、I-131が転移リンパ節・遠隔転移巣に取り込まれても、縮小するとは限りません[甲状腺分化癌(乳頭癌・濾胞癌)の2/3は放射線抵抗性]。
- I-131 治療抵抗性の甲状腺分化癌(乳頭癌・濾胞癌)の平均生存期間は、2.5~3.5年とされます。
I-131 放射線治療(内照射)に外部からの放射線照射(外照射)を併用すれば、治療効果は増します[Int J Mol Sci. 2017 Jun 17;18(6):1292.](第65回 日本甲状腺学会 O2-4 局所進行甲状腺分化癌に対する術後補助的外部放射線治療の傾向スコア解析を用いた治療成績)。
I-131 放射線治療(内照射)が効きにくい局所残存病変の制御には外照射の方が有効だからです[Crit Rev Oncol Hematol. 2013 Apr;86(1):52-68.][Int J Radiat Oncol Biol Phys. 2002 Mar 1;52(3):784-95.]。
頸部放射線照射(外照射)により
- 頸動脈壁が損傷して破綻出血をおこしやすくなります(carotid blowout syndrome)[Int J Radiat Oncol Biol Phys. 2021 May 1;110(1):147-159.]。
- 放射線誘発性アテローム性動脈硬化症を引き起こします。頸動脈狭窄の発生率は、頭頸部癌の放射線治療を受けた患者の18〜38%。放射線誘発性アテローム性動脈硬化症はカラードプラー超音波検査で検出でき、頸動脈血管形成術とステント留置術の血管内治療が第一選択。[Radiother Oncol. 2014 Jan;110(1):31-8.]
- 特に、甲状腺癌が頸動脈浸潤していると、病変の壊死・縮小・それに伴う感染などから頸動脈破裂をおこします。[BMJ Case Rep. 2021 Nov 30;14(11):e246084.]
放射性ヨウ素(I-131)放射線治療・I-131 アジュバント治療の問題点①放射線治療では甲状腺ホルモン剤中止による甲状腺機能低下症で心不全・うつ悪化、腎機能低下(低Na、高K血症、I-131排泄遅延で被曝量増加)②治療前の厳重なヨード(ヨウ素)制限食は難③累積被曝量は半端ない④妊婦や妊娠の可能性があると禁忌。有害事象・合併症は①唾液腺障害;唾液分泌障害により口内乾燥、虫歯・舌炎、味覚障害②鼻涙管閉塞③胃腸障害④反回神経麻痺⑤男性不妊(精巣への放射線障害)⑥甲状腺クリーゼ⑦汎血球減少⑧肺線維症⑨2次発癌。
I-131,治療,アジュバント,放射性ヨウ素,心不全,ヨウ素制限食,有害事象,合併症,唾液腺障害,甲状腺
I-131 放射線治療・I-131 アジュバント治療には以下の問題点があります。
- I-131 放射線治療・I-131 アジュバント治療はI-131 診断シンチ(I-131 シンチグラフィー)とI-131 アブレーション治療の3倍量以上の放射性ヨウ素(I-131)を使用します。30 mCiを超える場合、体内の放射線量が基準を下回るまで(30μSv/hr以下)の数日間は、放射線遮断・放射性下水処理ができる放射線治療専用個室に入院が必要(I-131 アブレーション治療の社会的問題点)。
- I-131 放射線治療前の約1カ月間、および放射線治療専用個室を退出して確認のI-131 シンチグラフィー(I-131 治療シンチ)が終わるまでは、甲状腺ホルモン剤(チラーヂンS)を中止するため、甲状腺機能低下症になります。倦怠感、むくみ、体重増加、体温低下などの症状、心不全・うつ悪化、腎機能低下(低ナトリウム血症、高カリウム血症)による放射性ヨウ素(I-131)の排泄遅延と被ばく量増加がおこります。治療後にホルモン剤を再開すると改善しますが、一番の問題は心不全の危険です。若くて甲状腺以外問題ない人なら難なく乗り越えられますが、元々、心機能に問題ある方には命の危険が生じます。
- 治療前3週間(少なくとも治療前2週間)からの厳重なヨード(ヨウ素)制限食は極めて重要だが、大多数の食品はヨード(ヨウ素)を含んでいるため、かなり難しい。
- 放射性ヨウ素(I-131) の合併症
-
放射線治療専用個室を退出後も、周囲への被曝を軽減するため、バセドウ病アイソトープ治療後と同じ指導が必要。
- 胎児への影響から妊婦や妊娠の可能性がある女性には禁忌です。乳汁にも放射性ヨード(I-131)が排泄されるため授乳もできません。しかし、この治療が原因で不妊が生じる事はないと言われています。
-
有効であれば、半年あるいは1年ごとに治療を繰り返すので、累積被ばく量は半端ではありません。(しかし、癌細胞を、せん滅しなければ命は無いため止む得ません。)
甲状腺分化癌(乳頭癌・濾胞癌)に対する放射性ヨード内用療法(I-131 アブレーション治療・I-131 アジュバント治療・I-131 放射線治療)で認められる有害事象(合併症)は、
- 唾液腺(耳下腺・顎下腺)障害:放射性ヨウ素(I-131)は唾液腺(耳下腺・顎下腺)にも取り込まれ、組織を破壊します。唾液分泌障害により、つばが出ず、口内乾燥、虫歯・舌炎、味覚障害をおこします。
①急性唾液分泌障害は回復する場合と永続的唾液分泌障害に移行する場合
②急性期症状がなく、永続的な唾液分泌障害になる場合
がありますが、放射性ヨウ素(I-131)治療を何度も繰り返し、積算投与量が増えると永続的唾液分泌障害になる確率は上がります。
放射性ヨウ素療法後の口腔ケアが重要です[Am J Med Sci. 2021 Jan;361(1):8-13.]。
- 二次性後天性鼻涙管閉塞[Curr Eye Res. 2021 Sep;46(9):1320-1324.]
- 嘔気(吐き気)と嘔吐:(ベータ線とは異なる)ガンマ線を高レベルで浴びると、一般的な放射線障害を起こします。嘔気(吐き気)などの放射線宿酔は一時的なものですが、放射性ヨード(I-131)治療を何度も繰り返すと永続的な胃腸障害になります。体重あたりの放射性ヨウ素(I-131) 投与量が多い程、症状が強く、放射性ヨウ素(I-131)大用量使用時は50~67%、低用量使用時は4%におこります。
胃潰瘍、胃炎があると、わずかな嘔気(吐き気)でもマロリーワイス症候群(Mallory-Weiss syndrome)に至る事があります(J Nucl Med. 1997 Nov;38(11):1831.)
- 反回神経麻痺:放射性ヨウ素(I-131)そのもので反回神経麻痺を引きおこすとは考えにくく、すでに反回神経あるいはその周囲に甲状腺分化癌の浸潤があって、それが崩壊する際に麻痺がおきると考えられます。
片側の反回神経が甲状腺癌の浸潤で麻痺し、もう片側が放射性ヨード内用療法後に麻痺すると両側性反回神経麻痺になり、自力呼吸できなくなります。気管切開して人工呼吸器の装着無しでは生きられません。
(第57回 日本甲状腺学会 P2-074 放射性ヨウ素内用療法後に反回神経麻痺を発症した甲状腺乳頭癌の1例)
- 永続的な男性不妊(精巣への放射線障害)
- 甲状腺クリーゼ
- 汎血球減少(白血球・赤血球・血小板すべてが減少);臨床的に問題となるような高度の汎血球減少は極めてまれとされます。しかし、①放射性ヨウ素(I-131) の累積投与量が多い②広範な骨転移により骨髄造血機能が、既に低下している③骨髄への照射線量(骨転移に対する放射線外照射)が多いなどで、高度の汎血球減少が起こり得ます。
- 肺線維症
- 2次発癌
- かなり稀ですが、副甲状腺への放射線障害で副甲状腺機能低下症[J Clin Endocrinol Metab. 2016 Jun;101(6):2284-99.]
[Endocr Pract. 2010 Nov-Dec;16(6):1064-70.][Pediatr Blood Cancer. 2017 Nov;64(11).]
I-131 放射線治療を何回行うのか明確な規定は有りません。もちろん高い放射線量の放射性ヨウ素(I-131)を使用するので、合併症も考慮しながら、かつ甲状腺分化癌に対する治療効果を出さねばなりません。最初から遠隔転移巣が放射性ヨウ素(I-131)を取り込まず、たとえ取り込んでも、治療後の縮小も血清サイログロブリン値の低下もなければ早々に止めるしかありません。
神戸市立医療センター中央市民病院は関西でも屈指のI-131 放射線治療施設で、I-131 放射線治療を4回以上施行した後に中断した16例の臨床検討を報告しています。治療回数平均9.5±4.7回、治療中断理由は放射性ヨウ素(I-131) 集積著減8例・回数が多いため4例・挙児(妊娠)希望2例・酸素投与が不要になったため1 例・高齢のため1例。中断後の経過観察期間12.2±4.7 年(4-24 年)では4例が再発・増悪のためI-131 放射線治療を再開したそうです。(第57回 日本甲状腺学会 P1-088 131I 治療を4 回以上施行し治療中断した16 例の臨床的検討)
フランスの報告では、遠隔転移を有する甲状腺分化癌患者に対して累積投与量3.7-22 GBq(100-600 mCi)のI-131 放射線治療を行った場合、
- 治療開始後5年以上で約半数患者の転移巣がシンチグラフィー上で消滅
- 特に若年者、分化度の高い例で有効
- 転移巣がシンチグラフィー上で消滅した患者の7%が再発、10年生存率92%(非消滅例では19%)
との結果です(J Clin Endocrinol Metab. 2006 Aug;91(8):2892-9.)。そのため、累積投与量の上限を22 GBq(600 mCi)とする意見があります。
最近では、「放射線治療無効な分化型甲状腺癌」にネクサバール錠®・レンビマカプセル®が保険適応になったため、I-131 放射線治療が効かない症例に無理して繰り返す必要はなくなりました。
I-131 放射線治療抵抗性の原因
I-131 放射線治療抵抗性の原因として、甲状腺乳頭癌の
- BRAF V600E変異;ナトリウム-ヨウ素シンポーター(NIS)の発現低下に関与。放射性ヨウ素(I-131)を取り込みにくい[Eur J Endocrinol. 2015 Oct;173(4):525-40.][Thyroid Res. 2018 Oct 11;11:13.]
BRAF阻害剤・MEK阻害剤(ダブラフェニブ・トラメチニブ)併用投与でNIS発現が上昇するため[Surgery. 2020 Jan;167(1):56-63.]、これらを投与した後にI-131 放射線治療することが推奨されています[Eur Thyroid J. 2022 Jan 1;11(1):e210046.]。(※ヨーロッパでの話です)
- RET遺伝子再配列(変異でなく再配列)、RET融合遺伝子とも言う);放射性ヨウ素(I-131)を取り込むが効きにくい。[J Exp Clin Cancer Res. 2020 Nov 16;39(1):245.]
I-131 放射線治療抵抗性患者の臨床的特徴
I-131 放射線治療抵抗性患者の臨床的特徴は、I-131 放射線治療の効果 をご覧ください。
I-131 放射線治療抵抗性の判断
I-131 放射線治療抵抗性の判断基準は、まちまちでDECISION試験、SELECT試験などで統一されていません。単純明快な基準は、「3-4回 I-131 放射線施行した後の病変部増大」です。
がん・感染症センター都立駒込病院等の報告では、I-131 放射線治療を行った111名[年齢中央値60歳、乳頭癌:濾胞癌:乳頭癌+濾胞癌:低分化癌=53:53:3:2名、投与量中央値500mC(i 範囲;300-1250mCi)、初回投与前の遠隔転移部位 なし:肺:骨:肺+骨=19:43:39:10名]の内、I-131 放射線治療抵抗性と判断された患者は99名/111名(89%)で投与回数中央値は3回(範囲;1-12回)。
I-131 放射線治療効果継続群と抵抗性群の5年生存率100%/100%、10年生存率89.9%/61.7%(p=0.036)。
甲状腺関連の上記以外の検査・治療 長崎甲状腺クリニック(大阪)
長崎甲状腺クリニック(大阪)とは
長崎甲状腺クリニック(大阪)は日本甲状腺学会認定 甲状腺専門医[橋本病,バセドウ病,甲状腺超音波(エコー)検査など]による甲状腺専門クリニック。大阪府大阪市東住吉区にあります。平野区,住吉区,阿倍野区,住之江区,松原市,堺市,羽曳野市,八尾市,東大阪市,生野区,天王寺区,浪速区も近く。